Προσθήκη πυρηνόφιλων άνθρακα
Μια ευρεία ποικιλία πυρηνόφιλων άνθρακα προσθέτει στις αλδεϋδες και τέτοιες αντιδράσεις έχουν πρωταρχική σημασία στη συνθετική οργανική χημεία, επειδή το προϊόν είναι ένας συνδυασμός δύο σκελετών άνθρακα. Οι οργανικοί χημικοί μπόρεσαν να συγκεντρώσουν σχεδόν οποιοδήποτε σκελετό άνθρακα, ανεξάρτητα από το πόσο περίπλοκο, με έξυπνες χρήσεις αυτών των αντιδράσεων. Ένα από τα παλαιότερα και πιο σημαντικά είναι η προσθήκη αντιδραστηρίων Grignard (RMgX, όπου το Χ είναι άτομο αλογόνου). Ο Γάλλος χημικός Victor Grignard κέρδισε το Βραβείο Νόμπελ στη χημεία του 1912 για την ανακάλυψη αυτών των αντιδραστηρίων και των αντιδράσεών τους.
Η προσθήκη αντιδραστηρίου Grignard σε αλδεΰδη ακολουθούμενη από οξίνιση σε υδατικό οξύ δίνει αλκοόλη. Η προσθήκη στη φορμαλδεΰδη δίνει πρωτογενή αλκοόλη. Η προσθήκη σε αλδεΰδη άλλη από τη φορμαλδεΰδη δίνει δευτερογενή αλκοόλη.
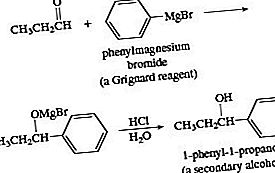
Ένα άλλο νουκλεόφιλο άνθρακα είναι το ιόν κυανιδίου, CN -, το οποίο αντιδρά με αλδεϋδες για να δώσει, μετά την οξίνιση, κυανοϋδρίνες, ενώσεις που περιέχουν μια ομάδα ΟΗ και CN στο ίδιο άτομο άνθρακα.
Η βενζαλδεϋδη κυανοϋδρίνη (μανδελονιτρίλιο) παρέχει ένα ενδιαφέρον παράδειγμα ενός μηχανισμού χημικής άμυνας στον βιολογικό κόσμο. Αυτή η ουσία συντίθεται από millipedes (Apheloria corugata) και αποθηκεύεται σε ειδικούς αδένες. Όταν απειλείται μια μιλιμπάδα, η κυανοϋδρίνη εκκρίνεται από τον αδένα αποθήκευσής της και υποβάλλεται σε καταλυόμενη από ένζυμο διαχωρισμό για την παραγωγή υδροκυανίου (HCN). Στη συνέχεια, η σαρανταποδαρούσα απελευθερώνει το αέριο HCN στο περιβάλλον του περιβάλλον για να αποτρέψει τους θηρευτές. Η ποσότητα του HCN που εκπέμπεται από μια μόνο χιλιοστόμπαρα είναι αρκετή για να σκοτώσει ένα μικρό ποντίκι. Το μαντελονιτρίλιο βρίσκεται επίσης σε πικρά αμύγδαλα και λάκκους ροδάκινου. Η λειτουργία του είναι άγνωστη.
Άλλες σημαντικές αντιδράσεις σε αυτήν την κατηγορία περιλαμβάνουν την αντίδραση Knoevenagel, στην οποία το νουκλεόφιλο άνθρακα είναι εστέρας με τουλάχιστον ένα α-υδρογόνο. Παρουσία μιας ισχυρής βάσης, ο εστέρας χάνει ένα α-υδρογόνο για να δώσει έναν αρνητικά φορτισμένο άνθρακα ο οποίος στη συνέχεια προσθέτει στον καρβονυλ άνθρακα μιας αλδεΰδης. Η οξίνιση που ακολουθείται από την απώλεια ενός μορίου νερού δίνει έναν α, β-ακόρεστο εστέρα.
Μια άλλη αντίδραση προσθήκης που περιλαμβάνει ένα νουκλεόφιλο άνθρακα είναι η αντίδραση Wittig, στην οποία μια αλδεΰδη αντιδρά με ένα φωσφοράνιο (επίσης αποκαλούμενο φωσφόρο υλίδιο), για να δώσει μια ένωση που περιέχει έναν διπλό δεσμό άνθρακα-άνθρακα. Το αποτέλεσμα μιας αντίδρασης Wittig είναι η αντικατάσταση του καρβονυλ οξυγόνου μιας αλδεΰδης από την ομάδα άνθρακα που συνδέεται με τον φώσφορο. Ο Γερμανός χημικός Georg Wittig μοιράστηκε το Βραβείο Νόμπελ του 1979 στη χημεία για την ανακάλυψη αυτής της αντίδρασης και την ανάπτυξη της χρήσης του στη συνθετική οργανική χημεία.
Ενώσεις που περιέχουν μία ομάδα τριμεθυλοσιλυλίου (-SiMe 3, όπου το Me είναι η ομάδα μεθυλίου, -CH 3) και ένα λιθίου (Li) άτομο επί του ιδίου ατόμου άνθρακα αντιδρούν με αλδεϋδες στον λεγόμενο αντίδραση Peterson για να δώσουν τα ίδια προϊόντα που θα να ληφθεί με αντίστοιχη αντίδραση Wittig.
Μετατόπιση στον α-άνθρακα
α-αλογόνωση
Μια α-υδρογόνου μιας αλδεΰδης μπορεί να αντικατασταθεί από ένα χλώριο (Cl), βρώμιο (Br) ή ιώδιο (Ι) άτομο όταν η ένωση υποβάλλεται σε επεξεργασία με Cl 2, Br 2, ή Ι 2, αντίστοιχα, είτε χωρίς ένα καταλύτη ή παρουσία όξινου καταλύτη.
Η αντίδραση μπορεί εύκολα να σταματήσει μετά την προσθήκη ενός μόνο ατόμου αλογόνου. Η α-αλογόνωση λαμβάνει χώρα πράγματι στη μορφή ενόλης (βλέπε παραπάνω Ιδιότητες αλδεϋδών: Ταυτομερισμός) της αλδεΰδης και όχι στην ίδια την αλδεϋδη. Η ίδια αντίδραση συμβαίνει εάν προστεθεί μια βάση, αλλά τότε δεν μπορεί να σταματήσει έως ότου όλα τα α-αλογόνα που συνδέονται στον ίδιο άνθρακα έχουν αντικατασταθεί από άτομα αλογόνου. Εάν υπάρχουν τρεις α-υδρογόνα επί του ιδίου άνθρακα, η αντίδραση προχωρά ένα βήμα παραπέρα, με αποτέλεσμα την διάσπαση ενός Χ 3 C - ιόντων (όπου το Χ είναι ένα αλογόνο) και το σχηματισμό του άλατος ενός καρβοξυλικού οξέος.

Αυτή η αντίδραση ονομάζεται αντίδραση αλοφορμική, διότι Χ 3 C - ιόντα αντιδρούν με νερό ή ένα άλλο οξύ που υπάρχει στο σύστημα για να παράγουν ενώσεις της μορφής Χ 3 CH, τα οποία ονομάζονται haloforms (π.χ., ΟΗΟΙ 3 ονομάζεται χλωροφόρμιο).

![Θαλάσσια καταστροφή από καταστροφή στο Eastland, Chicago River, Chicago, Illinois, Ηνωμένες Πολιτείες [1915] Θαλάσσια καταστροφή από καταστροφή στο Eastland, Chicago River, Chicago, Illinois, Ηνωμένες Πολιτείες [1915]](https://images.thetopknowledge.com/img/world-history/1/eastland-disaster-maritime-disaster-chicago-river-chicago-illinois-united-states-1915.jpg)











