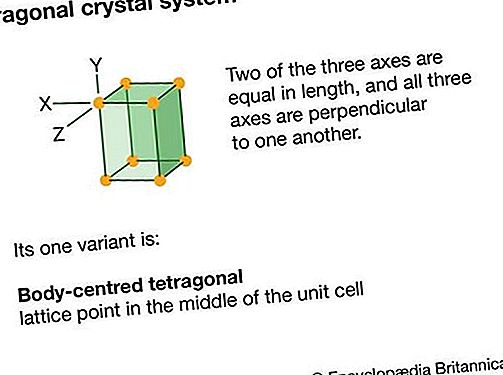
Φθόριο (F), το πιο αντιδραστικό χημικό στοιχείο και το ελαφρύτερο μέλος των στοιχείων αλογόνου ή Ομάδα 17 (Ομάδα VIIa) του περιοδικού πίνακα. Η χημική του δραστηριότητα μπορεί να αποδοθεί στην ακραία ικανότητά του να προσελκύει ηλεκτρόνια (είναι το πιο ηλεκτροαρνητικό στοιχείο) και στο μικρό μέγεθος των ατόμων του.
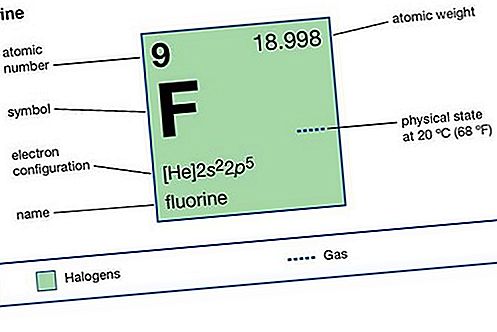
Ιδιότητες στοιχείου
| ατομικός αριθμός | 9 |
|---|---|
| ατομικό βάρος | 18.9984 |
| σημείο τήξης | −219,62 ° C (−363,32 ° F) |
| σημείο βρασμού | −188 ° C (−306 ° F) |
| πυκνότητα (1 atm, 0 ° C ή 32 ° F) | 1,696 g / λίτρο (0,226 ουγγιά / γαλόνι) |
| καταστάσεις οξείδωσης | −1 |
| διαμόρφωση ηλεκτρονίου | 1s 2 2s 2 2p 5 |
Ιστορία
Το περιέχον φθόριο ορυκτό φθοριούχο (ή φθορίτης) περιγράφηκε το 1529 από τον Γερμανό ιατρό και ορυκτολόγο Georgius Agricola. Φαίνεται πιθανό ότι το ακατέργαστο υδροφθορικό οξύ παρασκευάστηκε για πρώτη φορά από έναν άγνωστο Άγγλο υαλουργό το 1720. Το 1771 ο Σουηδός χημικός Carl Wilhelm Scheele έλαβε υδροφθορικό οξύ σε ακάθαρτη κατάσταση θερμαίνοντας φθοριούχο αλάτι με πυκνό θειικό οξύ σε γυάλινο αποστακτήριο, το οποίο διαβρώθηκε πολύ από το προϊόν; Ως αποτέλεσμα, δοχεία κατασκευασμένα από μέταλλο χρησιμοποιήθηκαν σε επόμενα πειράματα με την ουσία. Το σχεδόν άνυδρο οξύ παρασκευάστηκε το 1809 και δύο χρόνια αργότερα, ο Γάλλος φυσικός André-Marie Ampère πρότεινε ότι ήταν μια ένωση υδρογόνου με ένα άγνωστο στοιχείο, ανάλογο με το χλώριο, για το οποίο πρότεινε το όνομα φθόριο. Το φθοριούχο σπρέι στη συνέχεια αναγνωρίστηκε ως φθοριούχο ασβέστιο.
Η απομόνωση του φθορίου ήταν για μεγάλο χρονικό διάστημα ένα από τα κύρια ανεπίλυτα προβλήματα στην ανόργανη χημεία, και μόλις το 1886 ο Γάλλος χημικός Henri Moissan προετοίμασε το στοιχείο ηλεκτρολύοντας ένα διάλυμα υδροφθοριούχου καλίου σε υδροφθόριο. Έλαβε το βραβείο Νόμπελ Χημείας του 1906 για την απομόνωση του φθορίου. Η δυσκολία χειρισμού του στοιχείου και των τοξικών του ιδιοτήτων συνέβαλε στην αργή πρόοδο της χημείας φθορίου. Πράγματι, μέχρι τον Δεύτερο Παγκόσμιο Πόλεμο το στοιχείο φάνηκε να είναι εργαστηριακή περιέργεια. Στη συνέχεια, ωστόσο, η χρήση εξαφθοριούχου ουρανίου στο διαχωρισμό των ισοτόπων ουρανίου, μαζί με την ανάπτυξη οργανικών ενώσεων φθορίου βιομηχανικής σημασίας, έκανε το φθόριο βιομηχανική χημική ουσία σημαντικής χρήσης.
Εμφάνιση και κατανομή
Το φθόριο που περιέχει ανόργανο αργυραδάμαντα (φθορίτη, CAF 2) έχει χρησιμοποιηθεί για αιώνες ως ρευστοποιητής (παράγοντα καθαρισμού) σε διάφορες μεταλλουργικές διεργασίες. Το όνομα fluorspar προέρχεται από το λατινικό fluere, «to flow». Το ορυκτό στη συνέχεια αποδείχθηκε ότι είναι πηγή του στοιχείου, το οποίο επομένως ονομάστηκε φθόριο. Οι άχρωμοι, διαφανείς κρύσταλλοι φθορίου εμφανίζουν μπλε απόχρωση όταν φωτίζονται και αυτή η ιδιότητα είναι επομένως γνωστή ως φθορισμός.
Το φθόριο βρίσκεται στη φύση μόνο με τη μορφή των χημικών του ενώσεων, εκτός από τις ιχνοποσότητες του ελεύθερου στοιχείου στο φθοριούχο αλάτι που έχει υποβληθεί σε ακτινοβολία από το ράδιο. Δεν είναι ένα σπάνιο στοιχείο, αποτελεί περίπου το 0,065 τοις εκατό του φλοιού της Γης. Τα κύρια ανόργανα άλατα που περιέχουν φθόριο είναι (1) φθοράνθρακας, τα αποθέματα των οποίων εμφανίζονται στο Ιλλινόις, Κεντάκι, Ντέρμσαϊρ, νότια Γερμανία, νότια Γαλλία και Ρωσία και η κύρια πηγή φθορίου, (2) κρυόλιθος (Na 3 AlF 6), κυρίως από τη Γροιλανδία, (3) φθοροαπατίτης (Ca 5 [PO 4] 3 [F, Cl]), ευρέως διανεμημένος και περιέχει μεταβλητές ποσότητες φθορίου και χλωρίου, (4) τοπάζι (Al 2 SiO 4 [F, OH] 2), ο πολύτιμος λίθος, και (5) λεπιδολίτης, ένας μαρμαρυγία καθώς και συστατικό των οστών και των δοντιών των ζώων.