Διάχυση
Εξετάστε το σύστημα που περιγράφεται παραπάνω στον υπολογισμό της πίεσης αερίου, αλλά με την περιοχή Α στο τοίχωμα του δοχείου να αντικατασταθεί με μια μικρή οπή. Ο αριθμός των μορίων που διαφεύγουν από την οπή στο χρόνο t είναι ίσος με (1/2) (N / V) v z (At). Σε αυτήν την περίπτωση, οι συγκρούσεις μεταξύ μορίων είναι σημαντικές και το αποτέλεσμα ισχύει μόνο για μικροσκοπικές τρύπες σε πολύ λεπτά τοιχώματα (σε σύγκριση με τη μέση ελεύθερη διαδρομή), έτσι ώστε ένα μόριο που πλησιάζει κοντά στην τρύπα να περάσει χωρίς να συγκρουστεί με άλλο μόριο και απομακρύνεται. Η σχέση μεταξύ v z και μέσης ταχύτητας v̄ είναι μάλλον απλή: v z = (1/2) v̄.
Εάν συγκριθούν οι ρυθμοί για δύο διαφορετικά αέρια που εκτελούνται μέσω της ίδιας τρύπας, ξεκινώντας με την ίδια πυκνότητα αερίου κάθε φορά, διαπιστώνεται ότι πολύ περισσότερο ελαφρύ αέριο διαφεύγει από το βαρύ αέριο και ότι περισσότερο αέριο διαφεύγει σε υψηλή θερμοκρασία από ό, τι σε χαμηλή θερμοκρασία, άλλα πράγματα είναι ίδια. Συγκεκριμένα,
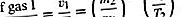
Το τελευταίο βήμα ακολουθεί τον ενεργειακό τύπο, (1/2) mv 2 = (3/2) kT, όπου (v 2) 1/2 προσεγγίζεται στο v, παρόλο που το v 2 και το (v̄) 2 διαφέρουν έναν αριθμητικό παράγοντα κοντά στην ενότητα (δηλαδή, 3π / 8). Αυτό το αποτέλεσμα ανακαλύφθηκε πειραματικά το 1846 από τον Graham για την περίπτωση της σταθερής θερμοκρασίας και είναι γνωστός ως ο νόμος της συλλογής του Graham. Μπορεί να χρησιμοποιηθεί για τη μέτρηση μοριακών βαρών, για τη μέτρηση της τάσης ατμών ενός υλικού με χαμηλή τάση ατμών, ή για τον υπολογισμό του ρυθμού εξάτμισης των μορίων από μια υγρή ή στερεή επιφάνεια.
Θερμική διαπνοή
Ας υποθέσουμε ότι δύο δοχεία του ίδιου αερίου αλλά σε διαφορετικές θερμοκρασίες συνδέονται από μια μικρή τρύπα και ότι το αέριο μεταφέρεται σε σταθερή κατάσταση. Εάν η τρύπα είναι αρκετά μικρή και η πυκνότητα αερίου είναι αρκετά χαμηλή ώστε να συμβεί μόνο η συλλογή, η πίεση ισορροπίας θα είναι μεγαλύτερη από την πλευρά της υψηλής θερμοκρασίας. Όμως, εάν οι αρχικές πιέσεις και στις δύο πλευρές είναι ίσες, το αέριο θα ρέει από την πλευρά χαμηλής θερμοκρασίας στην πλευρά υψηλής θερμοκρασίας για να προκαλέσει την αύξηση της πίεσης υψηλής θερμοκρασίας. Η τελευταία κατάσταση ονομάζεται θερμική διαπνοή και το αποτέλεσμα σταθερής κατάστασης ονομάζεται θερμομοριακή διαφορά πίεσης. Αυτά τα αποτελέσματα προκύπτουν απλώς από τη φόρμουλα συλλογής, εάν ο ιδανικός νόμος για το αέριο χρησιμοποιείται για την αντικατάσταση N / V με p / T.
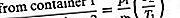
Όταν επιτυγχάνεται σταθερή κατάσταση, οι ρυθμοί διάχυσης είναι ίσοι, και έτσι
Αυτό το φαινόμενο διερευνήθηκε για πρώτη φορά πειραματικά από τον Osborne Reynolds το 1879 στο Manchester, Eng. Μπορεί να προκύψουν σφάλματα εάν η πίεση του αερίου μετρηθεί σε ένα δοχείο σε πολύ χαμηλή ή πολύ υψηλή θερμοκρασία συνδέοντάς το μέσω ενός λεπτού σωλήνα σε ένα μανόμετρο σε θερμοκρασία δωματίου. Μια συνεχής κυκλοφορία αερίου μπορεί να παραχθεί συνδέοντας τα δύο δοχεία με έναν άλλο σωλήνα του οποίου η διάμετρος είναι μεγάλη σε σύγκριση με τη μέση ελεύθερη διαδρομή. Η διαφορά πίεσης οδηγεί το αέριο μέσω αυτού του σωλήνα με ιξώδη ροή. Δυστυχώς, ένας κινητήρας θερμότητας με βάση αυτήν την κυκλοφορία έχει χαμηλή απόδοση.